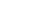我們為我們的醫療產品消費者帶來了好消息: 摩科醫用無塵車間通過EN ISO 13485:2016 通過 TUV SUD 認證. 我們現在擁有全球公認的信任和質量商標,以確保我們的客戶獲得安全, 可信的, 安全的, 和可持續的醫療設備提供可靠的解決方案.

什麼是國際標準化組織 13485 認證
ISO13485 是最終的質量管理體系 (質量管理體系) 醫療器械合格審定標準. 其主要目標是確保醫療產品和相關服務具有最佳質量,以實現最佳功能. 任何設計的公司或組織, 發展, 產生, 服務, 商店, 分發或安裝醫療資產需要滿足這些監管標準,然後才能向消費者部署其服務. 一如既往, MOKO讓我們的客戶’ 利益至上並符合這些標準.
該認證在全球範圍內得到認可. ISO13485 目前是 FDA 的強制性質量管理體系,此前美國提出了一項協調 ISO 的安排 1385:2016 和我們. 食品藥品監督管理局 21 病死率 820. ISO13485 認證可授予任何註冊組織, 只要它滿足監管要求,無論其規模如何. 然而, 證書不能頒發給一個人,因為它不是個人標準.
由於 ISO13485 不是產品的既定標準, 它並不決定醫療產品的質量. 反而, 這是目標組織應遵循的基於產品的標準.
醫療器械質量管理體系
醫療器械質量管理體系 (質量管理體系) 是一個有組織的系統,包括設計中涉及的程序和過程的標準要求, 原型製作, 製造業, 供應, 和醫療設備的存儲. 由於 ISO 不認可或證明任何公司符合其要求, 它授權 TUV SUD 等其他組織進行認證. 所以, 國際標準化組織 13485, 這是全球公認的醫療器械行業質量管理體系, 只是概述了公司獲得 ISO 所需的安全和資格標準 13485 TUV SUD 認證.
因此, 任何公司獲得TUV SUD認證, 它必須展示其提供不斷滿足客戶需求的醫療設備和解決方案的能力’ 和必要的監管要求.
新版ISO 13485 認證— ISO 13485:2016 以之前的 ISO 為基礎 9001 通過增加更多的監管要求. 這個新版本是在 3 月 1 日建立的, 2016, 並帶來了技術進步和全球需求演變的組合 12 年.
在那裡面 13485 對比. 國際標準化組織 13485 認證
大多數人與 EN 和 ISO 這兩個術語發生衝突,有時會陷入兩者的十字路口, 想知道採用或遵守哪些標準. 為了區別EN ISO 13485 來自國際標準化組織 13485, 我們需要了解 EN 標準和 ISO 標準的含義.
EN標準也被稱為歐洲協調標準. 他們的目的是確認符合歐洲 CE 禁令的重要監管要求. 這意味著必須將現有的 ISO 安全標準納入 EN 安全標準,而無需更改.
另一方面, ISO 安全標準是由標準化機構制定的一套監管要求——ISO 將被 TUV SUD 等第三方組織用來驗證公司的合規性,以便獲得認證.
一般來說, EN 標準不是由 EN 組織創建的獨立標準,而通常是由歐盟委員會協調的 IEC 或 ISO 安全標準 (歐共體).
例如, ISO 可以創建一個標準, 讓我們說ISO 45000 家庭——職業健康與安全. 然後, 如果歐盟成員國採用該標準, EC 必須將其作為 EN 標準發布,因為它是協調的. 當這件事發生時, 歐盟所有其他成員國隨後必須批准並採用這一統一標準,並廢除任何相互矛盾的國家標準. 協調後,ISO 標準必須以前綴 EN 重命名. 例如, 在那裡面 13485.
現在困難的部分已經過去了, 我們現在可以區分 EN ISO 13485 來自國際標準化組織 13485 認證. 在那裡面 13485 認證由受權批准公司符合統一 ISO 的組織提供 13485 歐盟地區標準. 相比之下, 國際標準化組織 13485 認證授予符合 ISO 標準的公司 13485 標準.
ISO13485認證流程
每個處理醫療器械的組織都必須經過嚴格的要求. 這是為了確保他們完全理解製造和提供醫療設備所需的過程. MOKO也不例外. 我們接受了 CB 的徹底審核 (認證機構) 在我們獲得 ISO 之前 13485 認證, 預計運行三年. 三年後, 我們將接受另一次審核以獲得重新認證.
這些要求會定期更新,因此需要在一段時間後重新認證.
認證過程分為 6 個步驟. 第一的, 組織需要記錄並展示其質量工廠以實施 QMS 的變更. 第二, 他們必須滿足其產品銷售地區的監管要求. 第三, 他們必鬚根據客戶的需求實施設計協議. 第四步要求組織在其質量管理過程中提交記錄和培訓文件. 在第五步, 認證委員會評估組織的風險管理過程, 這導致了認證審核的最後一步. 這是由醫療部門的特殊人員和 ISO 代理完成的. 審核完成後, 可能會建議幾個糾正計劃, 組織應該接受以頒發最終的 ISO13485 證書.
ISO 中的條款 13485 標準
1. (條款 4) 責任質量管理體系: 規定了需要認證的公司的一般要求和文件要求.
2. (條款 5) 管理職責: 概述質量方針, 管理評審, 規劃, 責任, 溝通 & 權威, 管理承諾, 和以客戶為中心.
3. (條款 6) 資源管理: 概述基礎設施, 人力資源, 工作環境 & 污染控制計劃, 資源來源/提供.
4. (條款 7) 產品實現: 概述生產 & 提供服務, 監控的控制 & 測量工具, 基於風險的產品實現方法, 設計 & 發展, 和客戶相關的流程.
5. (條款 8) 產品測量過程, 分析, 與改進: 概述監控 & 測量, 數據分析, 不合格品控制, 以及產品的改進.
如何選擇正確的安全標準
確保您不會因未能通過 ISO 或 EN 認證而被踢出市場, 你需要按照這些步驟. 他們將幫助您滿足設定的安全要求, 環境的, 和衛生標準.
1. 回答以下問題: 產品類型, 目標市場, 目標受眾/客戶, 銷售商品的國家, 最新的ISO/EN/IEC標準可參考, 適用於您的商品的州/地方立法.
2. 選擇正確的標準: 是否有任何州/地方 EN 或 ISO 或 IEC 標準適用於您的產品? 遵守您交易所在地區設定的所有行為準則.
3. 利用數字工具根據位置和產品類型等其他關鍵字查找要遵守的相關標準.
獲取 ISO 的優勢 13485 認證
這就是為什麼你應該得到你的 ISO 13485 醫療器械及相關產品認證:
1. 它增強了您的流程和程序’ 質量, 效力, 和透明度. 這將增加您對客戶的信任和您品牌的信譽.
2. 它證實了質量, 可靠性, 性能效率, 和您的醫療設備的安全.
3. 提高您的聲譽和消費者的滿意度
4. 作為貴公司的營銷工具
5. 沒有銷售退貨,因為您的產品符合標準質量和安全措施,足以打動和滿足您的客戶.
醫療設備可以平衡消費者的生死,這已不是什麼秘密. 考慮到這一點, MOKO始終力求在設計中通過質量管理審核, 開發和生產過程,以確保最終產品改善我們的消費者’ 生活. 這就是我們一次又一次通過 ISO13485 認證的原因.
除此之外, 我們已經成為 UL, RoHS, 國際標準化組織 14001 和 ISO I9001 以努力改善我們為客戶的整體運營.